Temps de lecture constaté 6,50’
Le séquençage approfondi du génome des divers variants du coronavirus Sars-CoV-2, le partage des données résultantes et la mise en place de protocoles de suivi de leurs émergences et de leurs devenirs constitueront des éléments essentiels pour collecter les informations nécessaires à l’adaptation des vaccins.
Lucy van Dorp, chercheuse en génomique microbienne et experte de l’évolution des pathogènes au sein de l’UCL de Londres, livre les informations connues sur ce variant qui fait tant peur partout dans le monde, aux côtés d’autres mutations appelées sans doute à se multiplier. Un article traduit et adapté par The Conversation France.
Un nouveau variant du coronavirus Sars-CoV-2, le virus responsable de la covid-19, pourrait être à l’origine d’une transmission accrue de cette maladie dans certains endroits du Royaume-Uni. En conséquence, le gouvernement britannique a mis en place, dans plusieurs régions, y compris à Londres, de nouvelles restrictions dites de « niveau 4 » (« Tier 4 »), plus drastiques. Les habitants des zones concernées n’ont pas passé Noël en compagnie de personnes extérieures à leur foyer. Ailleurs dans le pays, les réunions n’ont été autorisées que le jour même de Noël.
Le Premier ministre Boris Johnson et ses principaux conseillers scientifiques ont déclaré que suite à l’émergence de ce nouveau variant, la transmission de la maladie pourrait augmenter jusqu’à 70 % et que le taux de reproduction effectif pourrait s’accroître de 0,4 (le taux de reproduction est une estimation du nombre moyen d’individus que peut contaminer une personne infectée, le fameux R).
Que savons-nous de ce nouveau variant ?
La première annonce de ce nouveau variant détecté au Royaume-Uni, dénommé VUI–202012/01 ou lignage B.1.1.7, a été faite le 14 décembre 2020 par le ministre de la Santé britannique. L’information a ensuite été confirmée par Public Health England et le consortium britannique dédié au séquençage lié à l’épidémie de covid-19. Un examen des bases de données portant sur le Sars-CoV-2 a révélé que le premier échantillon contenant ce nouveau variant a été prélevé dans le comté du Kent le 20 septembre.
Le profil génétique – ou génome – de ce variant est porteur de 14 mutations, dont sept sont situées dans les régions codant pour la protéine Spike, qui sert de médiateur à l’entrée du virus dans les cellules humaines. Il s’agit d’un nombre de modifications relativement important par rapport aux nombreuses variantes en circulation dans le monde.
À ce jour, le génome de ce nouveau variant a été largement séquencé et les données partagées à partir d’échantillons recueillis principalement au Royaume-Uni. Il a toutefois également été trouvé au Danemark, ainsi qu’en Australie, à deux reprises. Un cas a aussi été signalé aux Pays-Bas. Il faut souligner que ces pays ont tous mis en place des politiques de séquençage du virus importantes, ce qui signifie qu’il est très possible que ces observations ne reflètent pas la véritable répartition mondiale de ce variant viral : il pourrait être présent ailleurs, mais ne pas être détecté faute d’un volume de séquençage suffisant. Nous en saurons plus à mesure que de nouveaux génomes seront séquencés et partagés.
Grâce au partage des données, à la surveillance génomique et aux résultats des tests covid-19 menés au Royaume-Uni, on constate que ce variant semble commencer à prendre le pas sur les autres. Il pourrait être responsable dans certaines régions du pays d’un nombre de cas de covid croissants, en particulier dans les endroits où ledit nombre augmente rapidement.
Dans ce type de situation, il est toujours très difficile de distinguer la cause de l’effet. L’augmentation de l’apparition de certaines mutations peut être due à l’augmentation de la fréquence des lignages viraux qui les portent, mais pas forcément parce qu’ils se transmettent mieux. Une explication alternative pourrait être que ces variants sont simplement présents dans des zones où la transmission est élevée, en raison de certaines activités humaines locales ou des politiques de santé publique qui y ont été mises en place, par exemple.
Mais bien que le succès de ce nouveau variant puisse s’expliquer de cette façon, les premières observations menées jusqu’à présent justifient le soin tout particulier apporté à sa caractérisation et sa surveillance, ainsi que la mise en place des interventions pour en enrayer la transmission.
Est-il plus dangereux ?
Le médecin en chef Chris Whitty a déclaré sans ambiguïté qu’il n’y avait pas de preuve à ce jour que ce variant du Sars-CoV-2 modifie la gravité de la maladie, que ce soit en termes de mortalité ou de sévérité des cas développés par les personnes infectées. Des travaux sont en cours pour le confirmer.
Comment se produisent les mutations des virus ?
Les mutations font naturellement partie de l’évolution des virus. Dans le cas du Sars-CoV-2, ces mutations peuvent résulter d’erreurs aléatoires lors de la réplication du virus. Ou être induites par des protéines antivirales présentes chez les personnes infectées. Ou encore survenir par recombinaison, une sorte de « brassage » génétique. Cependant, jusqu’ici aucun signe de recombinaison n’a été détecté pour le Sars-CoV-2.
La plupart des mutations virales sont généralement sans effet. Lorsque nous avions évalué les mutations ponctuelles qui ont affecté plus de 50 000 génomes viraux durant la première vague de la pandémie, nous n’en avons détecté aucune qui ait modifié de manière significative la capacité du virus à survivre et à se reproduire.
Il arrive cependant de temps à autre qu’une mutation, ou dans le cas présent une combinaison particulière de mutations, offre au virus un nouvel avantage. Si l’environnement épidémiologique le permet, les virus porteurs de ces combinaisons de mutations avantageuses risquent alors de voir leur fréquence augmenter dans la population, sous l’effet de la sélection naturelle.
Certaines des mutations du nouveau variant affectent la très importante protéine Spike.
D’où vient ce variant ?
Pour l’instant, nous ne le savons pas. Jusqu’à présent, les scientifiques n’ont pas identifié de virus étroitement apparentés à même d’étayer la théorie selon laquelle ce variant aurait été introduit dans le pays. Les profils de mutations observés sur la base des données actuellement disponibles plaident plutôt en faveur d’une longue période d’évolution adaptative, qui se serait très probablement passée au Royaume-Uni.
Des profils de mutation similaires à ceux-ci ont été observés lors de l’évolution du virus Sars-CoV-2 chez des patients chroniquement infectés, dont le système immunitaire est plus faible que la normale. L’hypothèse actuelle est qu’un tel scénario d’infection chronique, chez un seul patient, pourrait avoir joué un rôle dans l’émergence de ce variant. De nouvelles recherches vont être menées pour le préciser.
Combien de variants du Sars-CoV-2 avons-nous trouvés jusqu’ici ?
Il existe plusieurs milliers de lignages de Sars-CoV-2, lesquels diffèrent les uns des autres par un petit nombre de mutations en moyenne. La découverte de ce nouveau variant ne remet pas en cause le constat que les souches de Sars-CoV-2 actuellement en circulation dans le monde présentent une faible diversité génomique.
Si subtiles soient-elles, les mutations présentes dans les multiples lignages peuvent cependant être très utiles pour reconstituer les modèles de transmission. Au début de la pandémie, par exemple, au moins un millier d’introductions du Sars-CoV-2 au Royaume-Uni ont pu être identifiées par à leur attribution à tel ou tel lignage.
Pourquoi un variant est-il différent ?
Il est important de souligner que de nombreuses mutations présentes dans ce nouveau variant britannique ont déjà été observées dans d’autres variants du Sars-CoV-2 auparavant, parfois assez tôt dans la pandémie. Mais ce variant comporte un nombre et une combinaison de mutations inhabituels. Il a précédemment été montré que l’une de ces mutations, N501Y, augmente la liaison du virus aux récepteurs de nos cellules. N501Y a été séquencée pour la première fois dans un virus présent au Brésil en avril 2020. Elle est actuellement associée à un variant du Sars-CoV-2 dont la fréquence augmente également en Afrique du Sud – un lignage indépendant de B.1.1.7 qui mérite également d’être pris en compte.
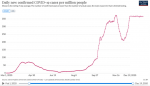
Le nouveau variant serait à l’origine de l’augmentation des taux de transmission au Royaume-Uni. Source : OurWorldInData, CC BY-SA
Les délétions [mutations génétiques] particulières identifiées dans la protéine Spike de B.1.1.7 sont apparues dans de multiples autres lignées du virus, à une fréquence croissante. Elles sont également observées dans les cas d’infections chroniques, où elles ont le pouvoir d’altérer l’antigénicité – c’est-à-dire la capacité du virus à être reconnu par les anticorps produits par le système immunitaire. Ces délétions sont également associées à d’autres mutations situées dans la région de liaison de la protéine Spike du coronavirus. C’est notamment le cas de mutations observées lors d’infections du vison d’élevage, ainsi que d’une mutation dont on sait qu’elle a joué un rôle dans la capacité du virus à échapper au système immunitaire chez l’être humain. Le nouveau variant B.1.1.7 possède également un gène ORF8 tronqué, or les délétions dans cette région ont été associées à une diminution de la gravité de la maladie.
L’effet fonctionnel de ces mutations et délétions, en particulier lorsqu’elles se trouvent combinées comme dans le cas de B.1.1.7, reste à déterminer. Le nombre élevé de mutations constatées dans ce variant particulier et la récente augmentation de sa prévalence, ainsi que l’importance biologique potentielle de certaines des mutations concernées, mettent l’accent sur la nécessité d’approfondir les recherches.
Quelles implications en matière de vaccin ? Sont-ils aussi efficaces à l’encontre de ce variant ?
Pour l’instant, nous ne le savons pas. Ce qui est rassurant, c’est que les vaccins entraînent une réponse anticorps large, dirigée contre l’ensemble de la protéine Spike. Leur efficacité ne devrait donc pas être entravée de manière significative par les mutations. Des essais visant à le confirmer sont en cours.
Toutefois, il existe un faisceau de preuves de plus en plus nombreuses indiquant que d’autres espèces de coronavirus saisonniers sont dans une certaine mesure capables d’échapper à l’immunité au fil du temps. Il n’est donc pas inconcevable que nous devions un jour actualiser les vaccins destinés à lutter contre la covid-19, comme nous le faisons pour ceux qui ciblent la grippe, afin de les adapter aux variants en circulation au moment de leur utilisation.
Il est trop tôt pour dire si cette situation se présentera. Ce qui est certain en revanche, c’est que le séquençage approfondi du génome des divers variants du coronavirus Sars-CoV-2, le partage des données résultantes et la mise en place de protocoles de suivi de leurs émergences et de leurs devenirs constitueront des éléments essentiels pour collecter les informations nécessaires à l’atteinte de cet objectif.